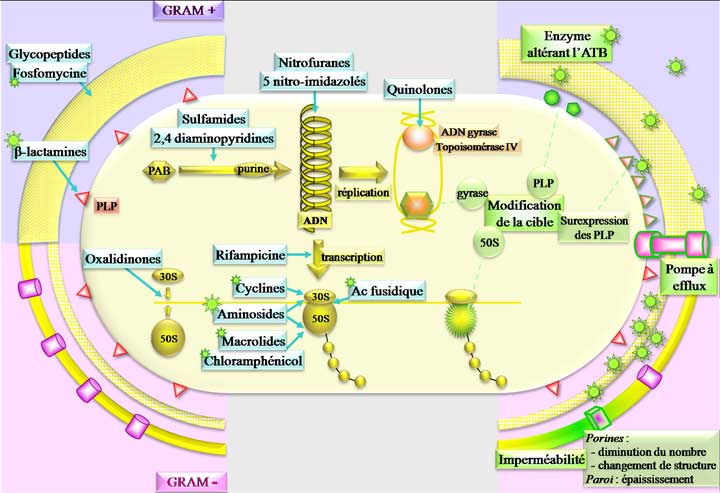
PLP : protéines liant les pénicillines PAB : acide para-amino-benzoïque NB : les antibiotiques bactériostatiques sont entourés en pointillés.
Famille d’ATB |
Principales
molécules |
Mécanismes d’action |
Mécanismes de
résistance |
| β-lactamines | Pénicillines : - Pénicilline V : Oracilline® - Pénicilline M : - Pénicilline A : - Pénicilline A +
inhibiteurs de b-lactamases (IBL) : - Amidino-pénicilline : Carboxy-pénicilline : Carboxy-pénicilline +
inhibiteur de b-lactamases : - Uréido-pénicilline : - Uréido-pénicilline
+ inhibiteurs de b-lactamases : Céphalosporines : Céphalosporines
de 2ème génération (C2G) : Céphamycines : - Céphalosporines
de 3ème génération (C3G) :
- Orales : Oxacéphème : Céphalosporine
à large spectre ou céphalosporine de 4ème génération (C4G) : Monobactams : Carbapénèmes : |
Inhibition de la synthèse du peptidoglycane par analogie de structure avec le substrat des PLP (D-ALA – D-ALA) et agissent donc par inhibition compétitive. Elles possèdent une activité bactéricide temps-dépendante. | Enzymes inactivatrices Pénicillinase (haut et bas niveau), TRI (pénicillinase résistant aux inhibiteurs), céphalosporinase, céphalosporinase déréprimée, b-lactamase à spectre élargie, carbapénémases …. Modification de la cible - Mutation sur les PLP : PLP2a des SARM PLP1a, 2x, 2a … des pneumocoques - Hyperproduction de PLP : PLP5 des entérocoques (E. faecium) Imperméabilité Mutation de la porine D2 (P. aeruginosa) Efflux P. aeruginosa |
| Glycopeptides | Vancomycine : Vancocine® Teicoplanine : Targocid® |
Inhibition de la synthèse du peptidoglycane par fixation sur le résidu D-ALA – D-ALA empêchant l’action des PLP par encombrement stérique | Modification de la cible Remplacement du résidu D-ALA – D-ALA par D-ALA – D-SER ou D-ALA – D-Lac |
| Fosfomycine | Fosfomycine : Fosfocine®, Uridoz®, Monuril® | Inhibition de la synthèse d’un précurseur du peptidoglycane par inhibition compétitive par analogie de substrat de la pyruvyl-transférase Le franchissement de la membrane plasmique se fait par un système de transport spécifique (glp T, uhp T) | Défaut de transport de l’antibiotique Enzymes inactivatrices Glutathion transférase, hydrolase … |
| Sulfamides et 2,4 diamino-pyridines | Sulfamides : Sulfadiazine : Adiazine® Sulfaméthisol : Rufol® 2,4 diaminopyridines Triméthoprime (+ sulfaméthoxazole) : Bactrim® Pyriméthamine (+ sulfadoxine) : Fansidar® |
Inhibition de la synthèse des bases puriques. Les sulfamides sont des analogues compétitifs de la dihydroptéroate synthétase. Les 2,4 diaminopyridines sont des analogues compétitifs de la dihydrofolate réductase. | Mutation de la cible Hyperproduction des enzymes cibles |
| Nitrofuranes | Nitrofurantoïne : Furadantine® Nifuroxazide : Ercéfuryl® |
Altération de l'ADN après réduction du groupement NO2 | |
| 5 nitro-imidazolés | Métronidazole : Flagyl® Métronidazole + spiramycine : Rodogyl® |
Coupure des brins d’ADN par formation de radicaux libres | |
| Quinolones | Quinolones de 1ère génération : Quinolones de 2ème génération ou fluoroquinolones : |
Inhibition des étapes de réplication et de transcription de l’ADN. Les quinolones forment un complexe avec l’ADN et la gyrase ou la topoisomérase IV (enzymes assurant le déroulement ou le surenroulement de l’ADN) Antibiotiques à activité bactéricide. | Mutation de la cible ADN gyrase (gyrA, gyrB) topoisomérase IV (parC, parE) Imperméabilité Déficit de l’expression des porines Efflux |
| Oxazilidones | Linézolide : Zyvoxid® | Inhibition de la phase d’initiation de la synthèse protéique | |
| Rifampicine | Rifampicine : Rifadine® | Inhibition de la transcription par inhibition de l’ARN polymérase ADN dépendante | |
| Cyclines | Tétracycline : Hexacycline® Doxycycline : Vibramycine® Minocycline : Minocine® Métacycline : Lysocline® Lymécycline : Tetralysal® Tigécycline : Tigacyl® |
Fixation irréversible sur la sous-unité 30S du ribosome et inhibition de la phase d’élongation de la synthèse protéique. Antibiotique à activité bactériostatique | |
| Aminosides | Streptomycine : Streptomycine® Kanamycine Tobramycine : Nebcine®, Tobrex® Gentamicine : Gentalline® Amikacine : Amiklin® Dibékacine : Débékacyl® Nétilmicine : Nétromycine® Spectinomycine : Trobicine® |
Fixation sur les sous-unités 30S ± 50S du ribosome et inhibition de toutes les étapes de la synthèse protéique : initiation, élongation, terminaison Activité bactéricide rapide et concentration dépendante Synergie d’action avec les antibiotiques détruisant la membrane | Enzymes inactivatrices - Aminosides phospho-transférases (APH) - Aminosides nucléotidyl-transférases (ANT) - Aminosides acétyl-transférases (AAC) Il existe plusieurs sous groupes de chaque enzyme. Imperméabilité Modification du LPS, diminution des porines Modification de la cible Modification du ribosome |
| MLS | Macrolides -
Macrolides à 15 atomes : -
Macrolides à 16 atomes : Lincosamides Synergistines Kétolides |
Fixation sur la sous-unité 50S du ribosome et blocage de l’élongation. Les macrolides et les lincosamides possèdent une activité bactériostatique Les synergistines sont bactéricides. | Modification de la cible Méthylation de la sous-unité 50S (erm) Enzymes inactivatrices Acétyl-transférase, hydrolase, acétylase Efflux |
| Phénicolés | Chloramphénicol : Tifomycine® Thiamphénicol : Thiophénicol® | Inhibition de la phase d’élongation de la synthèse protéique par fixation sur la sous-unité 50S du ribosome | Enzymes inactivatrices Chloramphénicol acétyltransférase |
| Acide fusidique | Acide fusidique : Fucidine® | Inhibition de la phase d’élongation de la synthèse protéique par formation d’un complexe avec le ribosome | |
| Polymyxines B et colistine | Colistine : Colimycine® | Altération de la membrane plasmatique par formation de pores |